자연살상세포 활성화로 간암 치료 효과 기대
 약학대학 서영거 교수 연구팀(사진)이 서울대 약학대학 이정원 교수 연구팀과 공동으로 연구한 논문이 지난 1월 22일, 네이처 포트폴리오 출판사의 생화학‧분자생물학(상위 0.8%) 및 세포생물학(상위 2.2%) 분야 저명한 국제학술지인 ‘신호 전달 및 표적 치료, Signal Transduction and Targeted Therapy(Impact factor, 40.8, 2023 JCR)’에 게재되는 연구 성과를 이루었다.
약학대학 서영거 교수 연구팀(사진)이 서울대 약학대학 이정원 교수 연구팀과 공동으로 연구한 논문이 지난 1월 22일, 네이처 포트폴리오 출판사의 생화학‧분자생물학(상위 0.8%) 및 세포생물학(상위 2.2%) 분야 저명한 국제학술지인 ‘신호 전달 및 표적 치료, Signal Transduction and Targeted Therapy(Impact factor, 40.8, 2023 JCR)’에 게재되는 연구 성과를 이루었다.
한국인의 간암 발병률은 여전히 높고 5년 생존율은 39%로 낮은 수준이다. 최근 개발되어 처방되고 있는 면역관문 억제제의 경우 간암 치료 효능에 한계가 있는 가운데, 서영거 교수 연구팀은 간암 치료의 새로운 가능성을 제시했다.
간암 조직에서 특정 단백질(TMF4SF5)이 면역세포의 기능을 억제하는 기전을 밝혀내고, 이를 차단하는 새로운 치료제를 개발한 것이다.
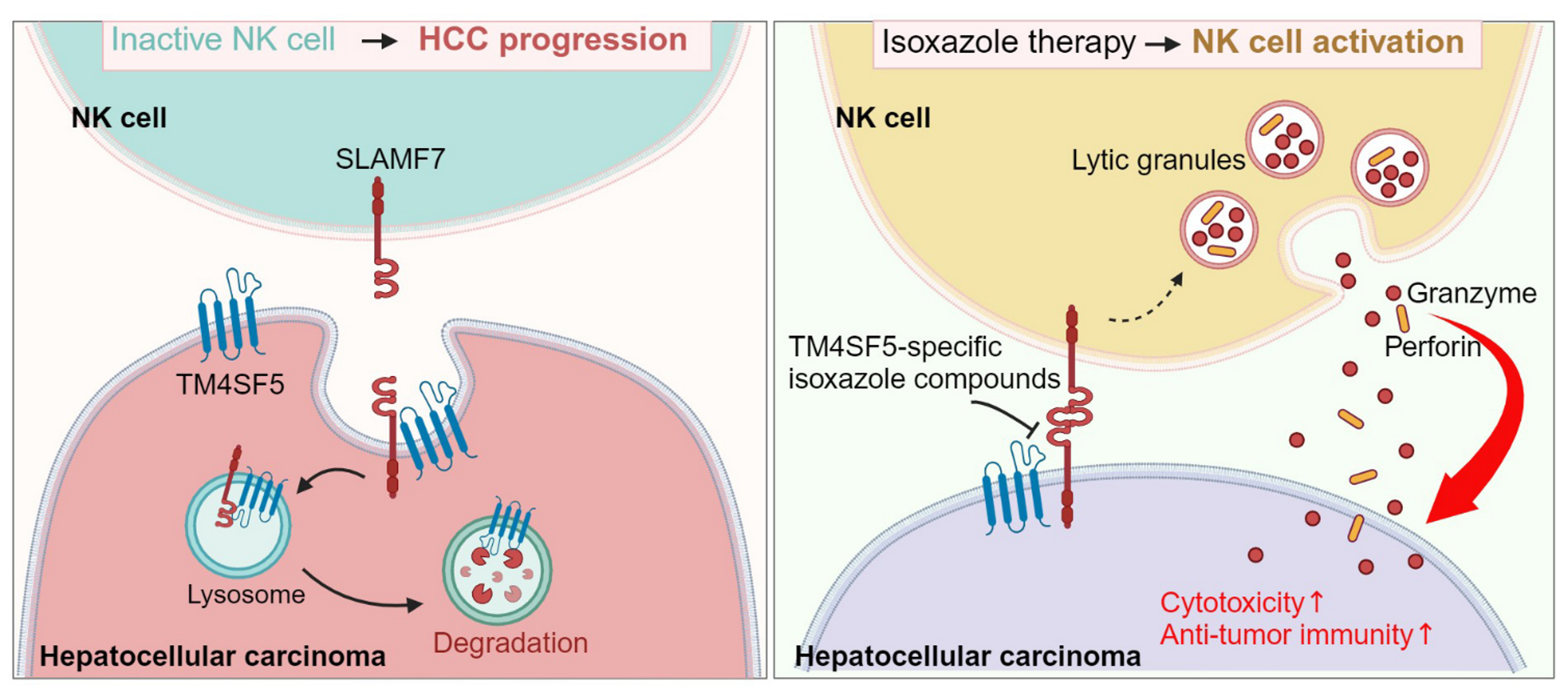
연구팀은 간암 조직에서 TM4SF5 단백질이 자연살상세포(NK 세포)의 활성화 관문인 SLAMF7의 발현을 억제한다는 사실을 밝혀냈으며, 이를 해결하기 위해 TM4SF5와 SLAMF7의 결합을 차단하는 새로운 억제제(TMF4SF5-specific isoxazole-based small molecules, TSI)를 개발했다. TSI는 SLAMF7이 리소좀에서 분해되는 것을 막아 NK 세포의 항암 기능을 유지하도록 돕는데, 이를 통해 간암 치료제로서의 가능성을 확인했다.
실험 결과, TSI를 투여한 동물 모델에서 간암 성장 억제 효과가 나타났으며, SLAMF7 발현 증가도 확인되었다. 연구진은 이를 기반으로 면역항암제 개발의 새로운 방향을 제시했다.
이번 연구는 간암 조직에서 면역세포 활성 조절 기전을 규명하고, 이를 표적으로 한 새로운 면역항암제 개발 가능성을 제시한 점에서 의미가 크다. 서영거 교수 연구팀은 “향후 지속적인 연구를 수행하여 간암 신약 후보 물질 개발을 위해 도전하고자 한다”고 밝혔다.
[제공 : 차 의과학대학교 일반대학원]
© CHA University – 상업적 무단전재ㆍ재배포 금지
















![[한 주 한 편, 영화 추천] 더 기버 : 기억전달자 인간의 감정, 기억, 자유의지에 대하여](https://newsroom.cha.ac.kr/wp-content/uploads/2022/10/1920x1200-218x150.png)








